
Jak wykonać badanie genów BRCA1/2?
W NINIEJSZYM ARTYKULE PORUSZONO NASTĘPUJĄCE ZAGADNIENIA:
-
Jak przeprowadzić badanie BRCA?
-
Badanie tkanki nowotworowej (guza)
-
Badanie mutacji germinalnych z krwi
Jak przeprowadzić badanie BRCA?
Proste, przesiewowe testy na obecność mutacji germinalnych BRCA1/2 są dostępne od lat 90-tych i są wykorzystywane do dziś w badaniach przesiewowych. Wykrywają one tylko część mutacji najczęściej spotykanych w populacji polskiej. Dzięki metodzie NGS (Sekwencjonowanie Nowej Generacji), która jest dostępna od niedawna, możemy skanować całe geny w poszukiwaniu mutacji germinalnych, jak i somatycznych. Ta metoda pozwala na wykrycie większości mutacji w dużych genach, do których zaliczają się geny BRCA 1/21,2.
Mutacje w genach BRCA1/2 mogą być germinalne lub somatyczne3,4.
-
Mutacje germinalne występują w każdej komórce ciała, także w komórkach rozrodczych (plemniku lub komórce jajowej), dlatego ten rodzaj mutacji może być dziedziczony, a tym samym może informować o ryzyku rodzinnym5. Wykrycie mutacji germinalnej w genie BRCA nie oznacza jednak, że każda kobieta w rodzinie na pewno zachoruje na raka jajnika, informuje jedynie, że istnieje zwiększone ryzyko wystąpienia choroby4.
-
Mutacje somatyczne to spontaniczne zmiany genetyczne. Ten rodzaj mutacji może rozwinąć się w każdej komórce ciała, z wyjątkiem komórek germinalnych (rozrodczych). Jest to mutacja niedziedziczna. Aby ją wykryć, badaniu należy poddać tkankę nowotworową, a następnie w badaniu genetycznym z krwi wykluczyć charakter germinalny wykrytego wariantu6.
Badanie BRCA1/2 w materiale pobranym z guza analizuje DNA nowotworowe i identyfikuje zarówno mutacje germinalne, jak i somatyczne w genach BRCA1/2. Nie jest ono jednak w stanie jednoznacznie określić, czy dana mutacja ma charakter somatyczny czy dziedziczny. W przypadku wykrycia mutacji przeprowadza się badanie z krwi, aby określić, czy mutacja jest pochodzenia germinalnego2,7. Mutacje germinalne BRCA1/2 występują w ok. 13%-18% surowiczych raków jajnika o wysokim stopniu złośliwości, a mutacje somatyczne w ok.7%8.
Ponieważ badania krwi mogą wykryć jedynie mutacje pochodzenia germinalnego, ok. 7% pacjentów z nabytymi mutacjami somatycznymi w genach BRCA1/2 nie zostanie zidentyfikowanych w badaniu z krwi7,8.
Częstość występowania mutacji BRCA1/2 w raku jajnika1,9


Badanie tkanki nowotworowej (guza)
Badania molekularne materiału z guza są wykorzystane do identyfikacji zmian genetycznych w komórkach nowotworowych, które mogą być przyczyną rozwoju nowotworu10. Tkanki utrwalone w formalinie zatopione w parafinie (FFPE), potocznie nazywane bloczkami, są rutynowo przygotowywane w jednostkach diagnostyki patomorfologicznej w większości szpitali i są powszechnie wykorzystywane do wielu różnych badań7,10. Dzięki postępowi w dziedzinie sekwencjonowania następnej generacji (NGS) tkanki FFPE mogą być obecnie wykorzystywane w badaniach molekularnych11.
Badanie BRCA1/2 w materiale pobranym z guza analizuje DNA nowotworowe i identyfikuje zarówno mutacje germinalne, jak i somatyczne w genach BRCA1/2. Nie jest ono jednak w stanie jednoznacznie określić, czy dana mutacja ma charakter somatyczny czy dziedziczny. W przypadku wykrycia mutacji, przeprowadza się badanie z krwi, aby określić, czy mutacja jest pochodzenia germinalnego2,10.
Użyteczność badań z tkanki pobranej z guza rośnie wraz z rozwojem coraz większej liczby terapii celowanych. W badaniu deficytu rekombinacji homologicznej (HRD) również wykorzystuje się DNA wyizolowane z tkanki nowotworowej (z bloczka/FFPE), aby ocenić aberracje genomowe, które są charakterystyczne dla deficytu rekombinacji homologicznej12-14.
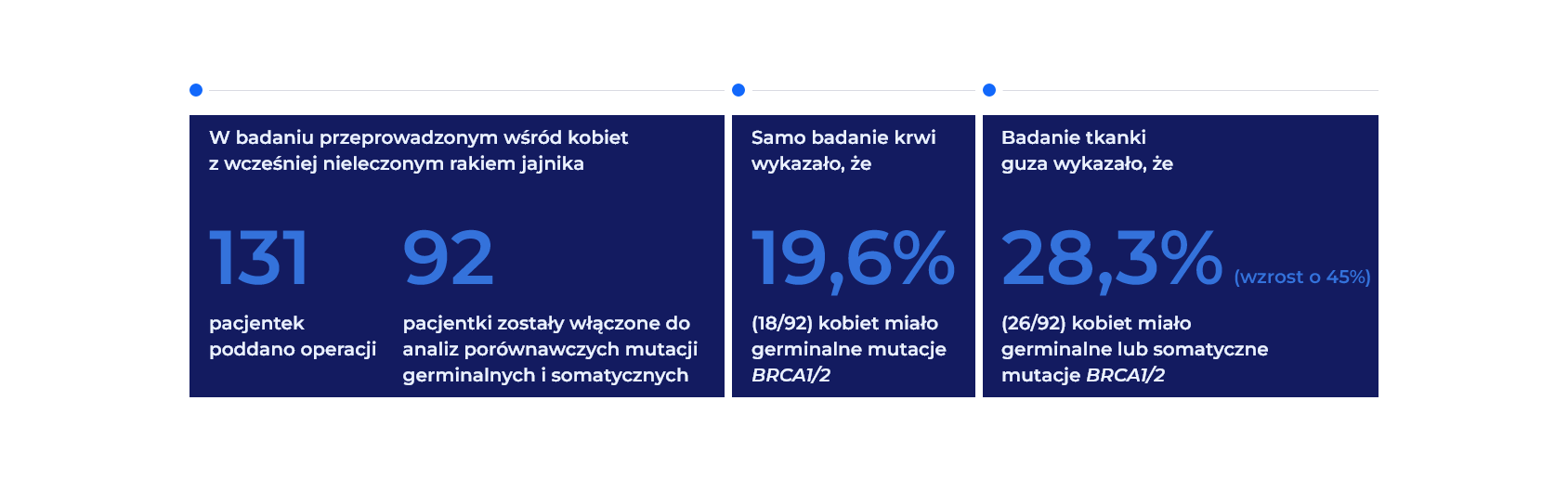
Do wykrycia somatycznych mutacji BRCA1/2 wymagane jest badanie materiału z guza15,16
W porównaniu z badaniem krwi, badanie materiału z guza może zwiększyć poziom wykrywalności mutacji BRCA1/2 u kobiet chorych na raka jajnika15.
Badanie mutacji germinalnych z krwi
Od pacjenta pobiera się próbkę krwi i wysyła do laboratorium w celu ekstrakcji DNA. DNA jest przetwarzane i badane w celu określenia obecności mutacji germinalnych BRCA7.
*Badanie materiału z guza – test BRCA – może ocenić DNA bezpośrednio z komórek nowotworowych, pobranych z biopsji, aby określić obecność mutacji. Badanie BRCA1/2 w materiale pobranym z guza analizuje DNA nowotworowe i identyfikuje zarówno mutacje germinalne jak i somatyczne. Nie jest ono jednak w stanie jednoznacznie określić, czy dana mutacja ma charakter somatyczny czy dziedziczny. W przypadku wykrycia mutacji przeprowadza się badanie z krwi, aby określić, czy mutacja jest pochodzenia germinalnego2,7.
Badanie NGS (Next-Generation Sequencing – Sekwencjonowanie Nowej Generacji)
Dziedzina badań genetycznych u chorych z rozpoznaniem raka jajnika rozwinęła się na przestrzeni ostatnich lat. Początkowo sekwencjonowano pojedyncze geny, co było pracochłonne i kosztowne16. Wraz z postępem technologii NGS wprowadzono panele wielogenowe, które pozwalają na szerszą ocenę genetyczną, szybszy proces badania, większą przepustowość, a przy tym optymalizują koszty procesu diagnostycznego17. Istotne klinicznie sekwencje genów docelowych zostały włączone do paneli genów NGS, zapewniając skuteczne narzędzia diagnostyczne do potencjalnej personalizacji terapii nowotworowych. Panele genów mogą oceniać wiele genów jednocześnie pod kątem specyficznych mutacji związanych z rakiem17.
Istnieje kilka metod badania mutacji w raku jajnika:4
-
Panel z ograniczoną liczbą genów: BRCA1 i BRCA2 – analiza sekwencji kodujących geny BRCA1 i BRCA217.
-
Panel wielogenowy*: wiele mutacji – bada status mutacji wielu genów za pomocą tylko jednej próbki i obejmuje BRCA1 i BRCA2, a także inne geny związane z rakiem9,17.
*Nie udowodniono, że badanie genów innych niż BRCA 1/2 z zastosowaniem panelu wielogenowego wspomaga podejmowanie decyzji o postępowaniu w przypadku nowo zdiagnozowanego raka jajnika.
Oprócz testów BRCA z zastosowaniem paneli NGS u pacjentów z rakiem jajnika stosuje się także badania sygnatur genomowych, które są związane z deficytem rekombinacji homologicznej (HRD)18.
Skróty i referencje:
BRCA1/2 – geny raka piersi; gBRCAm – germinalna mutacja BRCA; DNA – kwas dezoksyrybonukleinowy; NCCN – Narodowa Sieć ds. Nowotworów Kompleksowych® (NCCN®); NGS – sekwencjonowanie następnej generacji;
- Frey MK, Pothuri B. Homologous recombination deficiency (HRD) testing in ovarian cancer clinical practice: a review of the literature. Gynecol Oncol Res Pract. 2017; 22:4:4.
- Robson ME et al. American Society of Clinical Oncology policy statement update: genetic and genomic testing for cancer susceptibility. J Clin Oncol. 2010; 28: 893-901.
- Griffiths AJF et al. An Introduction to Genetic Analysis. 8th edition. New York: WH Freeman; 2000. Online: http://lgb.rc.unesp.br/biomol/literatura/Griffiths_8th.pdf [dostęp: 22.01.2024].
- Neff RT et al. BRCA mutation in ovarian cancer: testing, implications and treatment considerations. Ther Adv Med Oncol. 2017; 9: 519-531.
- National Cancer Institute. NCI Dictionary of Terms – germline mutation. Online: https://www.cancer.gov/publications/dictionaries/cancer-terms/def/germline-mutation [dostęp: 22.01.2024].
- National Cancer Institute. NCI Dictionary of Terms – somatic mutation. Online: https://www.cancer.gov/publications/dictionaries/cancer-terms/def/somatic-mutation [dostęp: 22.01.2024].
- Capoloungo E et al. Guidance Statement On BRCA1/2 Tumor Testing in Ovarian Cancer Patients. Sem in Oncol. 2017; 44(3): 187-197.
- Ratajska M et al. Detection of BRCA1/2 mutations in circulating tumor DNA from patients with ovarian cancer. Oncotarget. Online: https://doi.org/10.18632/oncotarget.20722 [dostęp: 22.01.2024].
- George A et al. Implementing rapid, robust, cost-effective, patient-centred, routine genetic testing in ovarian cancer patients. Sci Rep. 2016; 6: 29506
- Normanno N et al. Molecular diagnostics and personalized medicine in oncology: challenges and opportunities. J Cell Biochem. 2013; 114: 514-524.
- McDonough SJ et al. Use of FFPE-derived DNA in next generation sequencing: DNA extraction methods. PLoS One. 2019; 14(4): e0211400.
- D’Argenio V, Salvatore F. The role of the gut microbiome in the healthy adult status. Clinica Chimica Acta. 2015; 446: 221-225.
- Watkins JA et al. Genomic scars as biomarkers of homologous recombination deficiency and drug response in breast and ovarian cancers. Breast Cancer Res. 2014;16(3):211.
- Timms KM et al. Association of BRCA1/2 defects with genomic scores predictive of DNA damage repair deficiency among breast cancer subtypes. Breast Cancer Res. 2014;16(6):475.
- Pennington KP et al. Germline and somatic mutations in homologous recombination genes predict platinum response and survival in ovarian, fallopian tube, and peritoneal carcinomas. Clin Cancer Res. 2014; 20:764-75 [Tabela uzupełniająca 1].
- Kamps R et al. Next-Generation Sequencing in Oncology: Genetic Diagnosis, Risk Prediction and Cancer Classification. Int J Mol Sci. 2017; 18: 308.
- Lynce F, Isaacs C. How Far Do We Go With Genetic Evaluation? Gene, Panel, and Tumor Testing. Am Soc Clin Oncol Educ Book. 2016; 35: 72-e78.
- Mei R et al. Genome-wide detection of allelic imbalance using human SNPs and high-density DNA arrays. Genome Res. 2000; 10: 1126-1137.
Dowiedz
się więcej
Dowiedz się czym dokładnie jest BRCA1/2 i co zrobić, aby
zadbać o siebie i bliskich.